Therapia
Агранулоцитоз: от диагностики к выбору лечебной тактики
Агранулоцитоз (АЦ) — клинико-гематологический синдром, характеризующийся снижением уровня лейкоцитов (менее 1·109/л) за счет гранулоцитов (менее 0,75·109/л) и моноцитов, протекающий с тяжелыми инфекциями и некротической энтеропатией [1, 2].
В зависимости от патогенеза выделяют АЦ миелотоксический (цитостатическая болезнь) и иммунный, связанный с образованием антител к экзогенным антигенам — гаптенам (гаптеновый, лекарственный), или аутоиммунный (при коллагенозах, лимфомах, вирусных гепатитах). Гаптеновый АЦ (ГАЦ) — редкое заболевание, частота которого составляет 8–33 случая на 100 000 населения в год, имеет неблагоприятный прогноз вследствие развития тяжелых инфекционных осложнений. Смертность при ГАЦ ранее достигала до 90% случаев, в настоящее время составляет 20% [4]. В медицинской практике чаще встречается медикаментозный ГАЦ [2, 5].
Впервые АЦ был описан в 1922 г. W. Schultz [8] и независимо от него в 1931 г. R.R. Kracke [7]. Широкое применение цитостатической терапии (медикаментозной и лучевой), а также большого арсенала новых лекарственных средств привело к повышению частоты АЦ.
Этиология и патогенез
Выделяют три механизма развития АЦ [1]:
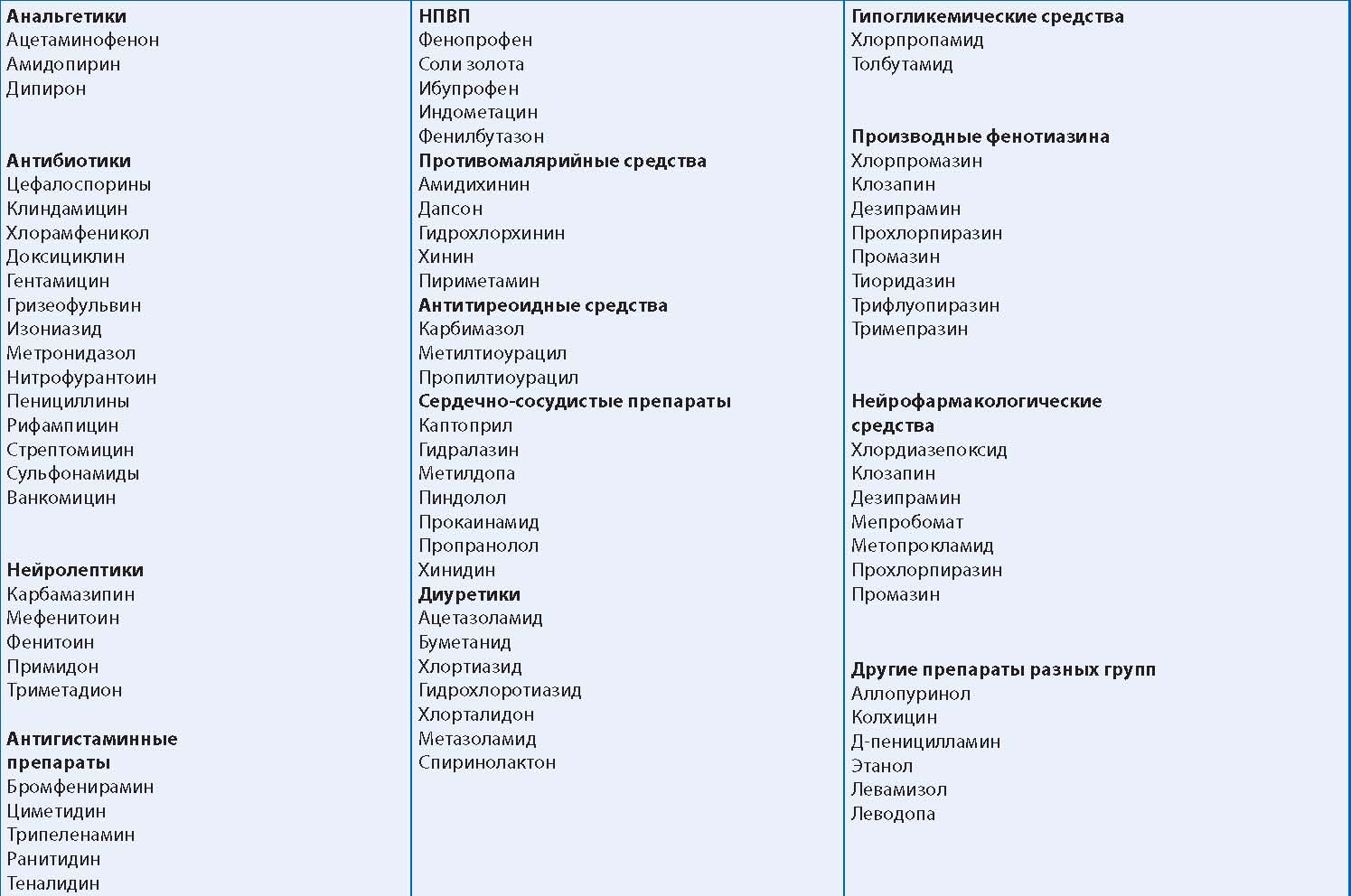
1. Лекарственный препарат может выступать в качестве гаптена и индуцировать синтез антител. Препараты, действующие по такому механизму, представлены в таблице. Чаще всего ГАЦ вызывают нестероидные противовоспалительные препараты (НПВП), сульфаниламиды, препараты золота, антитиреоидные и противомалярийные средства [5]. Препарат-гаптен соединяется с белками плазмы крови и приобретает свойства полноценного антигена, приводя к образованию антител к зрелым лейкоцитам или к клеткам — предшественницам гранулоцитопоэза. Антитела, связывающиеся с ним, обусловливают гибель гранулоцитов и, как следствие, развитие АЦ. В некоторых случаях антитела вызывают повреждение гранулоцитов без фиксации комплекса «препарат–белок плазмы» на их поверхности.
2. Прямое угнетение миелопоэза. По такому механизму АЦ может развиться при приеме карбамазепина и некоторых антибиотиков. В культуре клеток костного мозга эти препараты избирательно и дозозависимо угнетают миелоидный росток.
3. Прямое повреждение клеток микроокружения миелоидных предшественников в костном мозге.
Классификация АЦ
Наиболее удобной для практической работы является классификация, предложенная A. Distenfeld и соавторами [6]:
1. По этиологическому признаку:
– обусловленные приемом токсических препаратов (метамизол натрий, сульфаниламиды, бензольные производные);
– алиментарные (алиментарная токсическая алейкия);
– вызванные лучистой энергией;
– при системных поражениях соединительной ткани и кроветворной системы;
– при инфекционных процессах (сепсис, инфекционный эндокардит, флегмонозная ангина, гнойный отит и т. д.);
– при авитаминозах;
– идиопатические.
2. По патогенетическому признаку:
– гаптеновые;
– миелотоксические.
3. По клиническим проявлениям:
– псевдодифтерическая;
– язвенно-некротическая;
– номатозная;
– кишечно-некротическая энтеропатия.
4. По течению:
– острейшие или молниеносные;
– острые;
– подострые;
– рецидивирующие;
– циклические.
Клинические проявления АЦ
АЦ характеризуется острым или подострым началом, возникает через 7–14 дней после первого курса лечения препаратом, к которому сенсибилизирован организм, или через 1–2 дня после повторного его приема. Заболевание начинается ознобом, лихорадкой, артралгией. Одновременно развивается гранулоцитопения, которая через 12–24 ч перерастает в полный АЦ. Угрозу для жизни больного представляет септицемия. Степень инфекционного поражения связана с выраженностью АЦ.
При ГАЦ развитие болезни бурное. После приема препаратов, к которым имеется сенсибилизация, пациент отмечает нарастающую слабость, боль в горле, повышение температуры тела до 39–40 °С, появление и нарастание гнилостного (путридного) запаха изо рта (глоточно-ротовая форма). Нередко развиваются стоматит, ларингоспазм и асфиксия из-за скопления некротических пленок и отека гортани. Очень важным моментом, который может привести к ошибке в установлении диагноза, является то, что начальные проявления кишечно-некротической энтеропатии и поражение слизистых оболочек ротовой полости опережают появление лабораторных показателей АЦ.
Кишечная (тифоидная) форма проявляется развитием эрозий и язв слизистой оболочки желудка, тонкого и толстого кишечника, агранулоцитарного перитонита (некротическая энтеропатия). Эти проявления могут также сопровождаться геморрагическим компонентом, в том числе кишечным кровотечением.
Легочная (пневмоническая, гангренозная) форма возникает, как правило, при снижении уровня лейкоцитов в периферической крови менее 0,5·109/л. Быстро развивается пневмония, нередко с деструкцией легкого. Возможно атипичное течение пневмонии с отсутствием кашля, мокроты и типичных рентгенологических признаков, свойственных пневмонии. В этом случае заболевание проявляется высокой температурой тела, одышкой смешанного характера, при аускультации легких определяют крепитацию.
Установлено, что если сразу прекратить прием препарата, спровоцировавшего АЦ, то заболевание длится обычно 2–3 нед и не сопровождается развитием тяжелых осложнений. В крови постепенно появляются молодые формы гранулоцитов (миелоциты, метамиелоциты), увеличивается количество гранулоцитов. Нередко этому предшествует моноцитоз. В случаях развития язвенно-некротических поражений восстановление количества гранулоцитов и клиническое выздоровление происходят медленно.
Диагностические критерии АЦ
К критериям АЦ относятся:
1. Уменьшение количества гранулоцитов в периферической крови после 7 дней применения лекарственного препарата-гаптена или на 2–3-й день терапии при повторном его назначении.
2. Купирование клинических симптомов заболевания на фоне увеличения количества нейтрофильных гранулоцитов более 1,5·109/л через 1 мес после отмены препарата.
3. Изменения в клиническом анализе крови в виде лейко- и гранулоцитопении при неизмененном содержании эритроцитов и тромбоцитов.
4. Нормальное количество бластных клеток при исследовании костного мозга с умеренным повышением уровня плазматических клеток.
Таблица. Наиболее часто используемые препараты с потенциальным риском развития ГАЦ
Дифференциальная диагностика
Дифференциальный диагноз проводят в первую очередь с псевдонейтропенией, миелодиспластическим синдромом, острой лейкемией и др.
Псевдонейтропения характеризуется кратковременной нейтропенией вследствие перехода циркулирующих клеток в маргинальный пул. Транзиторную нейтропению наблюдают в течение 2 ч после введения препаратов рекомбинантного гранулоцитарного макрофагального колониестимулирующего фактора (Г-КСФ), фактора некроза опухоли (ФНО), поскольку под действием указанных препаратов увеличивается экспрессия нейтрофильными гранулоцитами СД11б/СД18, повышается их хемотаксическая активность и происходит перемещение из циркулирующего в маргинальный пул.
Миелодиспластический синдром — гетерогенная группа заболеваний, которые имеют клональный характер и характеризуются неэффективным гемопоэзом, проявляются цитопеническими изменениями периферической крови при гиперклеточном костном мозге, резистентностью к лечению. Наиболее частый признак миелодиспластического синдрома — рефрактерная анемия. У ряда больных можно обнаруживать признаки моно, би- или трехлинейной цитопении.
Дифференциальную диагностику миелодиспластического синдрома необходимо проводить также с В12-дефицитной анемией, сублейкемическим миелозом, пароксизмальной ночной гемоглобинурией, хронической миелоидной лейкемией. Характерной, но не обязательной чертой заболевания является пролиферация бластных клеток с исходом в дальнейшем в острый лейкоз.
Данные о заболеваемости миелодиспластическим синдромом в Украине практически отсутствуют. Это обусловлено тем, что в качестве самостоятельной нозологической формы этот синдром только недавно включен в МКБ-10.
При острой лейкемии выявляют трехростковое нарушение гемопоэза, увеличение количества бластов в костном мозге, наличие положительной реакции на специфические ферменты в бластных клетках.
При АЦ, в отличие от хронической нейтропении при аплазии костного мозга различного генеза, гиперспленизме и гепатогенной нейтропении, снижение концентрации нейтрофильных гранулоцитов происходит быстро, что приводит к развитию инфекционных осложнений в случае, если агранулоцитоз длится свыше 3 нед.
АЦ при цитостатической болезни практически всегда сопровождается тромбоцитопенией, лимфопенией и менее значимой ретикулоцитопенией. Развитие панцитопении при этом состоянии является дозозависимым осложнением.
Лечение АЦ
Лечебные мероприятия при АЦ любой этиологии должны включать:
1. Устранение этиологического повреждающего фактора и срочную госпитализацию больного в бокс (лучше в гематологическое отделение).
2. Создание асептических условий — изоляция, ультрафиолетовое облучение палат, тщательный уход за кожей и слизистыми оболочками. Подкожные и внутримышечные инъекции для предотвращения развития абсцессов следует заменить внутривенными.
3. Назначение антибиотиков широкого спектра действия (цефалоспорины II–III поколения, гентамицин по 80 мг/сут) и флуконазола (150 мг/сут).
4. При наличии вторичной вирусной и микозной инфекции применяют противовирусные препараты (ацикловир), амбазон, а также иммуноглобулин в дозе 0,5 г/кг через день или 3 раза в неделю до нормализации показателей гемограммы.
5. При некротической энтеропатии рекомендован перевод больного на парентеральное питание с обеспечением достаточной суточной энергетической ценности (30 ккал/кг и больше). Объем вводимых растворов должен составлять 40 мл/кг в сутки. Длительное парентеральное питание требует подключения эмульсионных растворов липидов, обладающих высокой энергетической ценностью. При проведении полного парентерального питания необходим контроль за центральным венозным давлением, диурезом, содержанием электролитов и глюкозы в крови.
6. Назначение препаратов гранулоцитарного колониестимулирующего фактора (КСФ). Благодаря их использованию средняя продолжительность лечения и сроки выздоровления больных значительно уменьшаются по сравнению с таковыми при терапии без применения КСФ. Сейчас в Украине представлены две формы КСФ: ленограстим и филграстим. В последнее время появились работы о применении в лечении больных с АЦ гемопоэтических стволовых клеток [5].
7. При аутоиммунном и иммунном АЦ назначают глюкокортикостероиды. Они уменьшают выраженность синдрома клеточного гиперкатаболизма. Дозы подбирают индивидуально в зависимости от тяжести состояния (в среднем они составляют 120–200 мг преднизолона в сутки).
8. Средствами выбора при лечении цитостатического АЦ являются препараты рекомбинантных гемопоэтических факторов роста — Г-КСФ, ГМ-КСФ, интерлейкина-1 и интерлейкина-3 [3].
Прогноз
Прогноз при АЦ ухудшается в случае повторного применения препарата, вызвавшего заболевание. Однако в последние годы в связи с использованием рекомбинантных КСФ прогноз значительно улучшился. Важным является тщательно собранный лекарственный и аллергологический анамнез, что позволит установить механизм развития заболевания в каждом отдельном случае. Немаловажное значение имеют своевременное установление диагноза и назначение адекватной терапии. При соблюдении этих правил вероятность благополучного исхода заболевания значительно возрастает.
Профилактика
Профилактика АЦ сводится к осторожному применению препаратов, которые могут вызвать иммунный конфликт или депрессию гемопоэза (см. таблицу). При их применении необходимо проводить клинический анализ крови каждые 3 дня. Важно исключить возможность повторного применения препарата, вызвавшего АЦ в анамнезе, так как это может привести к летальному исходу.
В качестве иллюстрации приводим собственное наблюдение типичного течения гаптенового АЦ.
Пациентка Б., 34 лет, поступила в эндокринологическое отделение областной клинической больницы с жалобами на похудение (уменьшение массы тела за время болезни на 9 кг), головокружение, учащенное сердцебиение, раздражительность, плаксивость, тремор рук.
Считала себя больной в течение последних 4 мес, когда появились указанные жалобы. Лечилась в районной больнице по поводу тиреотоксикоза тиамазолом с положительным эффектом. Ухудшение состояния отметила в последние 2 нед.
При поступлении состояние больной среднетяжелое.
Рост 165 см, масса тела 56 кг, индекс массы тела 20,5 кг/м2. Кожа и слизистые оболочки обычной окраски. Артериальное давление 130/80 мм рт. ст. , пульс 120 в 1 мин.
Щитовидная железа увеличена (ІІІ ст.), эластичной консистенции, безболезненная при пальпации, при глотании легко смещается.
В позе Ромберга отмечено мелкое дрожание кистей. Патологические глазные симптомы отсутствовали.
При аускультации над легкими выслушивали везикулярное дыхание.
Границы сердечной тупости не изменены. Сердечная деятельность ритмичная, тоны звучные, чистые.
Язык чистый. Живот мягкий, безболезненный. Печень пальпировали у края правой реберной дуги. Нижний полюс селезенки не пальпировался.
На основании клинических данных и результатов дополнительных методов исследования больной был установлен диагноз: диффузное увеличение щитовидной железы ІІІ степени, тиреотоксикоз среднетяжелого течения в стадии декомпенсации.
В общем анализе крови: эритроциты 4,1·1012/л, гемоглобин 132 г/л, тромбоциты 320·109/л, лейкоциты 7,5·109 /л (э. 3%; п. 4%; с. 63%; л. 25%; м. 5%). СОЭ 8 мм/ч.
В общем анализе мочи изменения отсутствовали.
Назначено лечение тиамазолом по 10 мг 3 раза в день, резерпином по 0,25 мг 3 раза в день, раствором Люголя 10 капель 2 раза в день, а также витамины В6 и В12.
В общем анализе крови через 1 нед после начала лечения изменения отсутствовали.
На 8-й день пребывания в отделении у больной температура тела повысилась до 39 °С, внезапно появились озноб, слабость, недомогание, боль в горле.
В общем анализе крови: снижение уровня лейкоцитов до 1,05·109/л и изменение в лейкоцитарной формуле (с. 8%; л. 39%, м. 3%, посчитано 50 клеток, обнаруженных на стекле). СОЭ 21 мм/ч. При повторном исследовании крови в тот же день лейкоциты 0,8·109/л (л. 99%; м. 1%), тромбоциты 302·109/л.
Больную осмотрел отоларинголог, который диагностировал фолликулярную ангину.
На основании полученных данных у больной заподозрен острый ГАЦ, ассоциированный с приемом тиамазола, в связи с чем этот препарат был отменен.
Приглашенный на консультацию гематолог подтвердил диагноз острого лекарственного (гаптенового) АЦ.
Больной назначена антибактериальная и противовоспалительная терапия: сультамицилин, ампициллин, преднизолон, γ-глобулин. Проведена инфузионная терапия, трансфузии лейкоцитно-тромбоцитарной взвеси.
Состояние больной оставалось тяжелым до 22-го дня пребывания в отделении. В общих анализах крови сохранялся АЦ, увеличение СОЭ до 50 мм/ч.
На 23-й день пребывания в отделении температура тела нормализовалась, исчезли боль в горле, появился аппетит.
В общем анализе крови: эритроциты 4·1012/л, гемоглобин 122 г/л, тромбоциты 228·109/л, лейкоциты 3,4·109 /л (п. 4%; с. 39%; л. 52%; м. 5%). СОЭ 24 мм/ч.
В костном мозге: промиелоциты 12%, миелоциты 60%, метамиелоциты 3%, палочкоядерные 12%, лимфоциты 9%, плазматические клетки 2%, бласты 2%.
На 30-й день пребывания в отделении больная переведена в хирургическое отделение для оперативного вмешательства по поводу тиреотоксикоза. Согласие на операцию получено. В общем анализе крови в день перевода: эритроциты 4,07·1012/л, гемоглобин 132 г/л, тромбоциты 312·109/л, лейкоциты 4·109 /л (п. 14%; с. 46%; л. 44%; м. 9%). СОЭ 8 мм/ч.
Особенностью данного наблюдения является ранняя диагностика ГАЦ и благоприятное его течение вследствие адекватной верификации заболевания и своевременно проведенной терапии.
Литература
- Алексеев, Г.А. Агранулоцитозы / Алексеев Г.А., Кассирский И.А. // Клиническая гематология. – 2-е изд. – М. : ГИМЛ, 1962. – С. 308–318.
- Воробьев, А.И., Руководство по гематологии / А.И. Воробьев, М.Д. Бриллиант. – М.: Медицина, 1995. – Т.1. – 410 с.
- Гайдукова, С. Агранулоцитоз / С. Гайдукова, С. Видиборець // Ліки України. – 2005. – № 10. – С. 21–27.
- Демидова, И. А. Случай успешной терапии гаптенового агранулоцитоза / И.А. Демидова, Е.О. Грибанова, В.Г. Савченко // Проблемы гематологии и переливания крови. – 1999. – № 2. – С. 52–53.
- Пивник, А. В. Гаптеновый агранулоцитоз: лечение гемопоэтическими ростовыми факторами / А.В. Пивник, В.Н. Тонкоглаз, Д.В. Бойко // Клин. медицина. – 2006. – № 3. – С. 55–59.
- Distenfeld A., Seiter K., Talavera T. et al. Argranulocytosis June 26, 2003 // www.Medicine.com.
- Kracke R. R. Recurrent argranulocytosis // Am. journ. clin. patholog. – 1981. – V. 1. – P. 385–389.
- Schultz W. Über eigenartige Halserkrankungen // Deutsch. Med. Wochenschr. – 1922. – V. 48. – P. 1495–1499.

